درک چگونگی ایجاد موانع محافظتی در باکتری های گرم منفی
به گزارش روابط پایگاه اطلاع رسانی علوم آزمایشگاهی ایران، محققان دانشگاه ییل Yale جزئیات جدیدی را در مورد چگونگی ایجاد موانع محافظتی باکتری هایی مانند E. coli کشف کرده اند که به توسعه آنتی بیوتیک جدید کمک می کند.
باکتری های مقاوم به آنتی بیوتیک یک مشکل رو به رشد برای مبارزه با عفونت ها هستند. مبارزه با باکتری هایی که دارای یک لایه محافظ اضافی برای دیواره سلولی خود هستند - نوعی که با توجه به روش رنگ آمیزی استفاده شده برای شناسایی آن به عنوان (گرم منفی) شناخته می شود.
محققان دانشگاه ییل از طریق مطالعه جدیدی که تفاوت های ظریف و اهداف اضافی برای توسعه آنتی بیوتیک های جدید را آشکار می کند، در درک چگونگی تولید این لایه محافظ توسط باکتری ها پیشرفت کرده اند.
یافته های آنها در 18 آوریل در National Academy of Sciences منتشر شد.
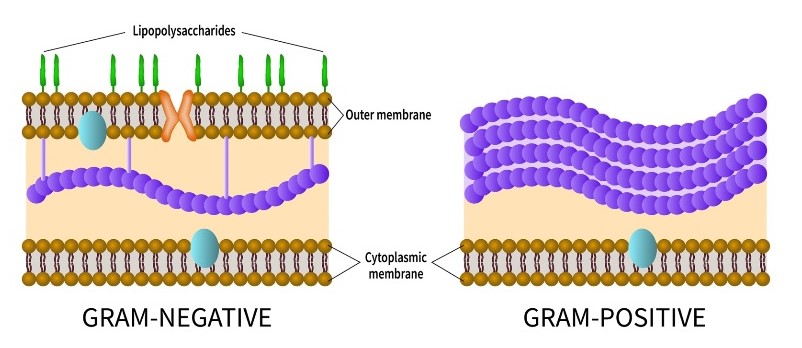
یکی از اجزای حیاتی این لایه محافظ، مولکولی به نام لیپوپلی ساکارید (LPS) است. باکتری ها به مقدار مشخصی LPS نیاز دارند. مقدار زیاد یا خیلی کم سلول را می کشد. تحقیقات قبلی از آزمایشگاه Wei Mi، استادیار فارماکولوژی در دانشکده پزشکی ییل، نشان داد که چگونه حسگرهای مولکولی موجود در E. coli تعادل مناسب تولید LPS را ایجاد می کنند.
در مطالعه جدید، محققان به بخش عمیق تری از این فرآیند که از تجمع LPS اضافی جلوگیری می کند، با هدف روشن کردن چگونگی اتصال پروتئینی به نام LapB و تحریک تخریب LpxC، آنزیمی که تولید LPS را آغاز می کند، پرداختند. محققان از میکروسکوپ الکترونی برودتی برای مشاهده ساختار مجتمع ایجاد شده هنگام اتصال این دو مولکول استفاده کردند.
می، نویسنده ارشد این مطالعه جدید، گفت: نگاه کردن به ساختار مستقیم ترین تجسم را از نحوه انجام این بخش از فرآیند ارائه می دهد. هنگامی که ساختار را دیدیم، تغییراتی در مولکول ها ایجاد کردیم تا ببینیم که چگونه بر اتصال تأثیر می گذارد، که به ما امکان می دهد تشخیص دهیم چه اجزایی برای LapB برای تشخیص LpxC ضروری است.
اما محققان همچنین در کمال تعجب دریافتند که LapB نه تنها مسئول تخریب LpxC است، بلکه از عملکرد آنزیم قبل از تخریب جلوگیری می کند.
اساساً، LapB قبل از اینکه آن را به صورت آشغال درآورد، LpxC را خاموش می کند. ما نمی دانیم چرا باکتری ها این کار را انجام می دهند، زیرا این کار اضافی به نظر می رسد، اما این چیزی است که اکنون به دنبال آن هستیم.
محققان حدس می زنند که این نقش دوگانه ممکن است در مورد انعطاف پذیری باشد. تخریب فرآیندی آهسته اما غیرقابل برگشت است، در حالی که مهار سریع و برگشت پذیر است. داشتن هر دو قابلیت ممکن است باکتری ها را قادر می سازد تا به تغییرات محیطی با سرعت بیشتری پاسخ دهند.





